Wichtiger Hinweis
Ich verfolge die Studienlage seit etwa 2023/2024 nicht mehr – schlichtweg aus Zeitgründen neben einem Vollzeitjob und anderen Interessen (z.b. die eigene Gesundheit) nicht möglich! Deswegen werde ich das Kapitel, obwohl ich es für sehr wichtig halte, so knapp wie möglich darstellen. Für aktuelle Infos bitte ich zu den entsprechenden Institutionen zu gehen, etwa dem Nationalen Referenzzentrum für postvirale Syndrome der MedUni Wien oder zur Physiotherapeutin Verena Hackl, spezialisiert auf Long Covid und MECFS (gut gemachte Webseite), siehe auch Neurologe Stingl (neurostingl.at) u.v.a – wie gesagt, ich habs nicht mehr im Blick, wo und welche Spezialisten es gibt. Der Blog wird diesbezüglich unvermeidbar veraltet sein.
Eine Liste meiner bisher gesammelten Studien gibt es am Ende dieser Seite.
Hintergrund
Long Covid (LC) ist ein Oberbegriff für die Langzeitschäden nach einer SARS-CoV2-Infektion. Die allgemein gehaltene Verwendung des Begriffs behindert jedoch exakte epidemiologische Forschung, Diagnostik und Therapieansätze (Leonard A. Jason 2024). Es kommt zu regelmäßigen Fehlinterpretationen bei Erhebungen in der Bevölkerung. Daher ist eine exakte Terminologie wichtig. Zu beachten ist aber, dass LC ein Spektrum ist, mit fließenden Übergängen verschiedener Subtypen und Symptomen.
Viele Studien zu Beginn der Pandemie fußten auf selektiven Teilnehmergruppen (z.B. Selbsthilfegruppen), sehr breiter Definition und unbekannten Risikofaktoren. Entsprechend kamen hohe Inzidenzraten zustande und vermeintlich keine Korrelation zur Krankheitsschwere und Gesundheitszustand vor der Infektion.
Langjährige MECFS-Betroffenen wie Dr. Daniel Loy warnten schon im April 2020 auf Twitter und kritisierten die falsche Dichotomie der Krankheitsverläufe mit genesen oder tot (langer thread). Meine ersten Hinweise bekam ich durch Paul Garner, der im Mai 2020 seine persönlichen Erfahrungen schilderte und in Österreich gab es Ende April 2020 Warnungen an Taucher vor erhöhter Unfallgefahr nach einer Infektion.
Zu den Pionieren des Begriffs Long Covid zählte Elisa Perego et al. (2020) und Nisreen Alwan, Epidemiologin und selbst Betroffene, die frühzeitig dafür plädierte, die Schwere der Erkrankung nach der Krankheitsdauer zu definieren und nicht danach, ob jemand hospitalisiert werden muss (Nisreen Alwan 2020).
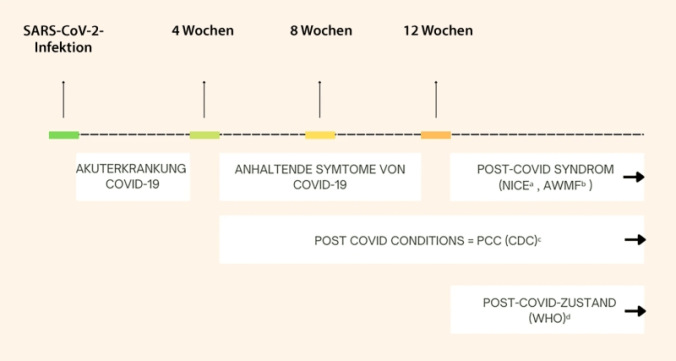
Die erste WHO-Definition gab es am 13. Februar 2021 und wurde am 06. Oktober 2021 aktualisiert. Seitdem wird LC im ICD-10 unter U09.9 (“post Covid-19 condition, nicht näher bezeichnet”) erfasst.
Hoffmann et al. (2024) definiert LC in drei Subtypen:
- anhaltend symptomatische Erkrankung
- durch Covid verursachte oder verstärkte Krankheiten
- post-akuter Covid-Zustand (postakutes Infektionssyndrom PAIS)
Long Covid Subtyp 1:
„Ein Spitalsaufenthalt wegen Covid sollte in jedem Fall verhindert werden, da stecken ja Schicksale dahinter.“ (Gesundheitsökonom Thomas Czypionka, STANDARD, 21.09.20)
Anhaltend symptomatische Erkrankung
- z.B. mit akutem Atemnotsyndrom (ARDS), schwere Lungenentzündung, Herzmuskelentzündung, multisystemischem Entzündungssyndrom (MICS),
- Symptome aufgrund von Organschäden bei schwerem Verlauf (z.B. Beteiligung von Gehirn, Herz, Nieren, Lunge) oder durch die Therapie (z.B. Beatmung, PICS) mit Symptomen, die bis zu 12 Wochen andauern.
- Nach 12 Wochen sollte es “anhaltende Spätfolgen von Corona” genannt werden.
Ein wesentlicher Fehler in der Risikokommunikation war so tun, als ob man wieder gesund aus dem Krankenhaus entlassen würde, wenn nur genügend freie Betten zur Verfügung stehen. Schwere Verläufe erhöhen grundsätzlich das Risiko für Spätfolgen, einerseits durch die Virusinfektion, andererseits durch die Behandlung selbst, insbesondere nach längerer Beatmungsdauer oder ECMO-Therapie auf der Intensivstation.
Sowohl Schäden durch Langzeitbeatmung als auch Organschäden treten gehäuft auf mit langwieriger Rehabilitation (Raman et al. 2020, Evans et al. 2022). LC ist deutlich wahrscheinlicher als nach milden Verläufen (Carfi et al. 2020, Munro et al. 2020, Arnold et al. 2020, Chou et al. 2021, Daughertly et al. 2021). Manche Patienten entwickeln nach der Hospitalisierung Atemwegssymptome, die Monate anhalten (Vijayakumar et al. 2022). Viele Betroffene müssen erneut ins Krankenhaus, die Sterblichkeit ist erhöht (Chopra et al. 2020, Ayoubkhani et al. 2021, Günster et al. 2021, ), auch kognitive Einschränkungen treten gehäuft auf ( Becker et al. 2021). Ältere Menschen mit Grunderkrankungen werden durch einen schweren Covid19-Verlauf noch kränker (Cohen et al. 2022).
Nach 3 Jahren hat sich bei den meisten Patienten die Lungenfunktion nahezu normalisiert, es gibt ein höheres Reinfektionsrisiko als bei Personen ohne LC und bei der Hälfte bleiben weiterhin Symptome bestehen (Zhang et al. 11/2023). Mehrere spezifische Plasmaproteine können als Biomarker für LC nach schweren Verläufen dienen (Liew et al. 2024).
Von schweren Verläufen sind tendenziell etwas häufiger Männer betroffen, rund ein Fünftel braucht mechanische Beatmung. Die Sterblichkeit liegt bei 14%.
Risikofaktoren für schwere Verläufe
- 65 Jahre und älter
- erhöhte Kreatin/Troponinwerte
- Lymphozytenmangel, Lungeninfiltrate.
- Hohe Viruslast und niedrige Antikörperwerte
- Ein Viertel der Überlebenden entwickelt Post-Covid-Symptome.
Impfungen verringern das LC-Risiko nach schwerem Verlauf (Birtolo et al. 2024).
Long Covid Subtyp 2
Durch Corona verursachte oder verstärkte Krankheiten
- Symptome für mehr als 4 Wochen, durch Verschlechterung bestehender chronische Krankheiten durch die Infektion und/oder erstmalig aufgetreten in zeitlicher Nähe zur Infektion
- z.B. Thrombosen, Embolien, Schlaganfall, Herzkreislauf-Erkrankungen, Asthma, atypische Lungenfibrose, Autoimmunerkrankung, Diabetes, Demenzsyndrome) und/oder verwandte erhöhte Risiken, z.B. Asthma bronchiale oder Lupus Erythematosus
Etwa ein Viertel aller älteren Post-Covid-Patienten erhält durch die Infektion eine neue Grunderkrankung (Bull-Otterson et al. 2022).
Long Covid Subtyp 3
post-akuter Covid-Zustand
- tritt häufig auch nach milden Infektionen auf
- nicht erklärbar durch andere Diagnosen wie LC-Subtyp 1+2
- Symptome dauern länger als drei Monate an
- Post-akut im Gegensatz zu “post Covid” betonen, dass es sich um ein post-akutes Infektionssyndrom (PAIS) handelt, das hier durch SARS-CoV2 verursacht wurde.
- z.B. post-exertional malaise (PEM), Dysautonomie (DA), posturales Tachykardiesyndrom (POTS), Dysregulation des Immunsystems, z.B. Mastzellenüberaktivierung (MCAS) und kognitive Beeinträchtigungen
Hierbei handelt es sich um das “klassische” LC, über das in den Medien am häufigsten berichtet wird. Es muss aber nicht zwangsläufig PEM als Leitsymptom auftreten – hier spricht man dann bei Erfüllung der CCC/IOM-Kriterien von MECFS (siehe Menüpunkt).
Die Unterscheidung von LC mit und ohne PEM ist ganz wesentlich für den Behandlungsansatz.
Ein chronischer Verlauf von [3] kann zu myalgic encephalomyelitis/chronic fatigue syndrome (MECFS) führen, dessen Leitsymptom PEM ist.
Postvirale Syndrome allgemein
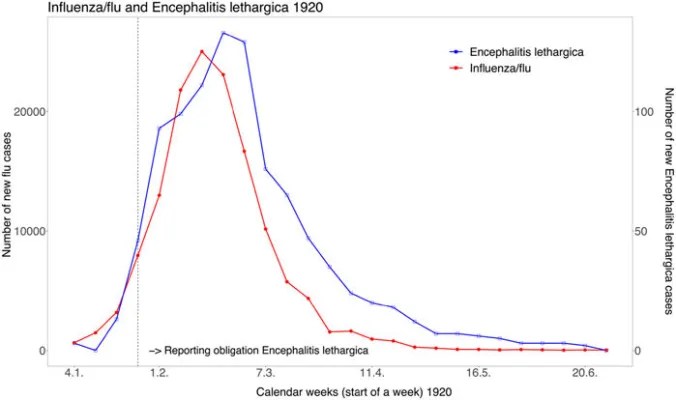
Eine gute Übersicht gibt es von Staub et al. (2024), der Schweizer Beispiele aus den Pandemien von 1890, 1918-20 und später bringt. Deutschlandfunk zum Thema (21.01.25)
Eine weitere Übersicht zu postviralen Fatigue-Syndromen gibt es von S Wessely (1991), bzw. George B. Stefano (2021). Auch nach der „Russischen Grippe“ gab es anhaltende Fatigue, Herzprobleme, Angsterkrankungen, neurologische Erkrankungen. Grunderkrankungen wurden oft durch die Influenza verschlechtert. Kinder litten vermehrt unter kognitiven Erkrankungen.
- Für Coronaviren allgemein sind sie schon lange bekannt (Robb and Bond 1979).
- Bereits nach SARS-CoV1 wurden Spätfolgen festgestellt (Leung et al. 2004, Gu et al. 2005, Lam et al. 2009, Wu et al. 2017, Li et al. 2023).
- Masern radieren das Immungedächtnis für andere Erkrankungen durch großen Verlust an Antikörpervielfalt aus (Mina et al. 2019, Petrova et al. 2019)
- Ebolaviren lösen Langzeitfolgen aus (Linda Geddes 2021, The Guardian).
- Chikungunya-Viren lösen LC-ähnliche Langzeitfolgen aus (Simon et al. 2021)
- Epstein-Barr-Viren können MECFS (Hickie et al. 2006) und zudem Multiple Sklerose auslösen (Bjornevik et al. 2022, Gottlieb et al. 2024, Vietzen et al. 2024), zudem können sie das Pfeiffersche Drüsenfieber auslösen (Kuri et al. 2020)
- Herpes Simplex Virus 2 könnte Alzheimer auslösen (Roberts et al. 2023)
- Herpes Zoster erhöht Alzheimer-Risiko (Eyting et al. 2023 preprint) und Schlaganfallrisiko (Paramesawaran et al. 2022), Gürtelrose-Impfung reduziert Demenzrisiko (Taquet et al. 2024)
- Influenzaviren, aber nicht die Impfung dagegen, können MECFS auslösen (Magnus et al. 2015)
- Verschiedene Viren erhöhen das Risiko für neurodegenerative Erkrankungen bis zu 15 Jahre nach einer einzigen Virusinfektion, besonders deutlich ist der Zusammenhang u.a. mit Influenza und begleitender Lungenentzündung (Blackhurst and Funk 2023, Levine et al. 2023)
- Die gute Nachricht: Impfungen verringern das Risiko für Alzheimer, Parkinson und andere Erkrankungen dieser Art (Lehrer and Rheinstein 2022).
Literatursammlung
Fachartikel
++++
Long Covid bei Kindern und Jugendlichen
+++
Prävalenz, Inzidenz und Follow-Up-Studien
++++
Risiko- und Biomarker (Ursachensuche)
++++
Diagnostik, Therapie und Medikamente
++++
Forschung und Kommentare
++++
Long Covid /MECFS und Behörden
++++
Long Covid und Lebensqualität
++++
Long Covid: Folgen für den Arbeitsmarkt
++++
Presse zu Long Covid/MECFS
You must be logged in to post a comment.